Tasa fotosintética y producción de biomasa por inoculación de Scleroderma sp. con diferentes concentraciones de NaCl en nogal pecanero
DOI:
https://doi.org/10.29312/remexca.v13i7.3024Palabras clave:
comportamiento de plántulas, medio estresante, micorrizasResumen
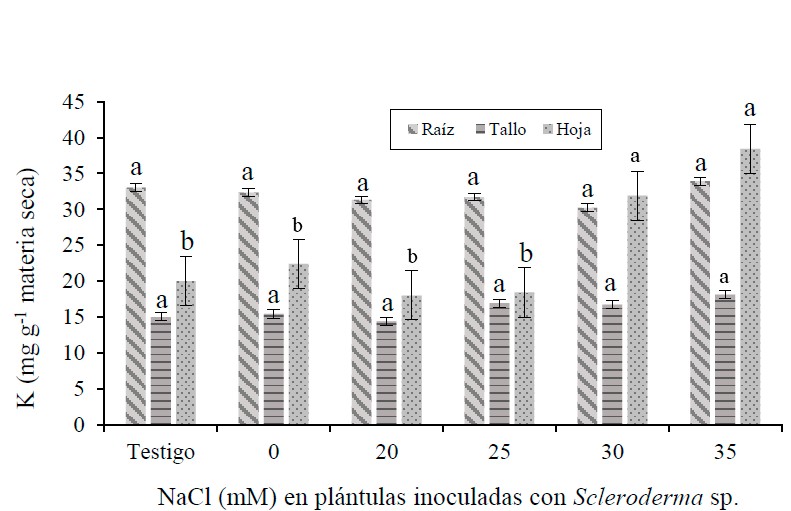
El nogal pecanero [Carya illinoinensis (Wangenh) K. Koch] es uno de los frutales establecidos en el norte de México, donde existe una superficie considerable de suelos con diferente grado de salinidad, a la cual el árbol es sensible. En plántulas inoculadas con Escleroderma sp., se avaluó el efecto de NaCl en concentraciones de 0, 20, 25, 30 y 35 mM, incluyendo un testigo sin inocular y sin NaCl. El experimento se realizó en la Unidad Regional Universitaria de Zonas Áridas en Bermejillo, Durango, México, en condiciones de invernadero. Las plántulas fueron regadas dos veces por semana, durante 2018. Las plantas inoculadas y bajo condición no salina, mostraron la mayor fotosíntesis y transpiración, seguida por las plántulas testigo. La concentración de Na+ en raíz, tallo y hoja fue menor en el testigo y en las plántulas inoculadas y sin NaCl. La concentración de K en plántulas inoculadas y bajo condición salina y no salina fue similar al testigo. La relación k/Na fue mayor en el testigo y en las plántulas inoculadas y bajo condición no salina y disminuyó a medida que incrementó la concentración de NaCl particularmente en raíz. Las plántulas testigo mostraron mayor peso seco en raíz tallo y hoja que las inoculadas con Scleroderma sp. y bajo estrés salino, pero fue menor que en las inoculadas con el hongo y bajo condición no salina. En plántulas bajo estrés salino de 20 y 35 mM, la disminución del peso seco fue de 8.5 y 47%, en comparación al testigo. Las plántulas de nogal inoculadas con Scleroderma sp. y bajo condición no salina, mostraron mejor respuesta fisiológica y de acumulación de biomasa y no bajo condición salina.
Descargas
Citas
Babuin, M.; Echeverria, M.; Menendez, A. and Maiale, S. 2016. Arbuscular mycorrhizal pecan seedlings alleviate effect of restricted water supply. HortScience. 51(3):212-215. Doi: https://doi.org/10.21273/hortsci.51.3.212.
Bandou, E.; Lebailly, F.; Muller, F.; Dulormne, M.; Toribio, A.; Chabrol, J.; Courtecuisse R.; Plenchette, C.; Prin, Y.; Duponnois, R.; Thiao, M.; Sylla, S.; Dreyfus, B. and Ba, A. 2006. The ectomycorrhizal fungus Scleroderma bermudense alleviates salt stress in seagrape (Coccoloba uvifera L.) seedlings. Mycorrhiza. 16(8):559-565. Doi: https://doi.org/10. 1007/s00572-006-0073-6.
Bassil, E.; Coku, A. and Blumwald, E. 2012. Cellular ion homeostasis: emerging roles of intracellular NHX Na+/H+ antiporters in plant growth and development. J. Exp. Bot. 63(16):5727-5740. Doi: https://doi.org/10.1093/jxb/ers250.
Behrozz, A.; Vahdati, K.; Rejali, F.; Lotfi, M.; Saadat, S. and Leslie, Ch. 2019. Arbuscular mycorrhiza and plant growth-promoting bacteria alleviate drought stress in walnut. HortScience. 54(6):1087-1092. Doi: https://doi.org/10.21273/HORTSCI13961-19.
Birhane, E.; Sterck, F. J.; Fetene. M.; Bongers, F. and Kuyper, T. 2012. Arbuscular mycorrhizal fungi enhance photosynthesis, water use effciency, and growth of frankincense seedlings under pulsed water availability conditions. Oecologia. 169(4):895-904. Doi: https://doi.org/10.1007/s00442-012-2258-3.
Bonito, G.; Brnneman, T. and Vilgalys, R. 2011. Ectomycorrhizal fungal diversity in orchards of cultivated pecan (Carya illinoinensis; Juglandaceae). Mycorrhiza. 21(7):601-612. Doi: https://doi.org/10.1007/s00572-011-0368-0.
Campos, V. A.; Arreola, A. J.; Trejo, C. R.; Borja, A.; López, S. y Hernández, R. 2017. Respuesta fisiológica, acumulación iónica y peso seco en portainjertos de nogal pecanero (Carya illinoinensis (wangenh) k. koch) desarrollados bajo condiciones de estrés salino. Interciencia. 42(11):744-749.
Chen, Z.; Zhou, M. X.; Newman, I. A.; Mendham, N. J.; Zhang, G. P. and Shabala, S. 2007. Potassium and sodium relations in salinised barley tissues as a basis of differential salt tolerance. Funct. Plant Biol. 34(2):150-162. Doi: https://doi.org/10.1071/FP06237.
Estrada, B.; Aroca, R.; Barea, J. and Ruíz, L. J. M. 2013. Native arbuscular mycorrhizal fungi isolated from a saline habitat improved maize antioxidant systems and plant tolerance to salinity. Plant Science. 201(1):42-51. Doi: https://doi.org/10.1016/j.plantsci.2012. 11.009.
Evelin, H.; Kapoor, R. and Giri, B. 2009. Arbuscular mycorrhizal fungi in alleviation of salt stress: a review. Ann. Bot. 104(7):1263-1280. Doi: https://doi.org/10.1093/ aob/mcp251.
Feng, G.; Zhang, F.; Li, X.; Tian, C. T.; Tanq, C. and Rengel, Z. 2006. Uptake of nitrogen from indigenous soil pool by cotton plant inoculated with arbuscular mycorrhizal fungi. Comm. Soil Sci. Plant Analysis. 33(19):3825-3836. Doi: https://doi.org/10.1081/ CSS-120015925.
Giri, B.; Kapoor, R. and Mukerji, K. G. 2003. Influence of arbuscular mycorrhizal fungi and salinity on growth, biomass and mineral nutrition of Acacia auriculiformis. Biol. Fertil. Soils. 38(3):170-175. Doi: https://doi.org/10.1007/s00374-003-0636-z.
Giri, B.; Kapoor, R. and Mukerji, K. G. 2007. Improved tolerance of Acacia nilotica to salt stress by arbuscular mycorrhiza, Glomus fasciculatum, may be partly related to elevated K/Na ratios in root and shoot tissues. Microbial Ecol. 54(4):753-760. Doi: https://doi.org/ 10.1007/s00248-007-9239-9. Guzmán, H. G.; Cortés, P. A.; Guzmán, D. L.; Ramírez, G. F. and Refugio, S. J. M. 2013. An emendation of Scleroderma, new records, and review of the known species in Mexico. Rev. Mex. Bio. 84(suplemento):S173-S191. Doi: https://doi.org/10.7550/rmb.31979.
Lee, S. H.; Calvo, P. M.; Chung, G. C. and Zwiazek, J. J. 2010. Role of aquaporins in root water transport of ectomycorrhizal jack pine (Pinus banksiana) seedlings exposed to NaCl and fluoride. Plant Cell Environ. 33(5):769-780. Doi: https://doi.org/10.1111/j.1365-3040.2009.02103.x
Li. J.; Bao, S.; Zhang, Y.; Ma, X.; Mishra, K. M.; Sun, J.; Sa, G.; Shen, X.; Polle, A. and Chen, S. 2012. Paxillus involutus strains MAJ and NAU mediate K+/Na+ homeostasis in ectomycorrhizal Populus×canescens under NaCl stress. Plant Physiol. Doi: https://doi.org/10.1104/pp.112.195370. 159(4): 1771-1786.
Lu, Y. W.; Wang, G. Q.; Meng, Q. J.; Zhang, W. H. and, Duan, B. L. 2014. Growth and physiological responses to arbuscular mycorrhizal fungi and salt stress in dioecious plant Populus tomentosa. Canadian J. Forest Res. 44(9):1020-1031. Doi: https://doi.org/10.1139/ cjfr-2014-0009.
Ma, X.; Sun, M.; Sa, G.; Zhang, Y.; Li, J.; Sun, J.; Shen, X.; Polle, A. and Chen, S. 2014. Ion fluxes in Paxillus involutus-inoculated roots of Populus×canescens under saline stress. 108(4):99-108. Doi: https://doi.org/10.1016/j.envexpbot.2013.11.016.
Miyamoto, S. and Nesbitt, M. 2011. Effectiveness of soil salinity management practices in basin irrigated pecan orchards. HortTechnology. 21(5):569-576. Doi: https://doi.org/10.21273/ HORTTECH.21.5.569.
Moreno, I. E.; Ojeda, B. C.; Avila, Q. G.; Prieto, G. B.; Parra, Q. R. and Anchondo, R. T. 2015. Sodium sulfate exposure slows growth of native pecan seedlings. Rev. Inter. Bot. Exp. 84(1):80-85. https://Doi:10.32604/phyton.2015.84.080.
Muhsin, T. M. and Zwiazek, J. J. 2002. Colonization with Hebeloma crustuliniforme increases water conductance and limits shoot sodium uptake in white spruce (Picea glauca) seedlings. Plant and Soil 238(2):217-225. Doi: https://doi.org/10.1023/A:1014435 407735.
Nguyen, M.; Calvo, P. M. and Zwiazek, J. 2006. Gas exchange and growth responses of ectomycorrhizal Picea mariana, Picea glauca, and Pinus banksiana seedlings to NaCl and Na2SO4. Plant Biol. 8(5):646-652. Doi: https://doi.org/10.1055/s-2006-924106.
Parvin, S.; Van, G. M.; Yeasmin, T.; Verbruggen, E. and Honnay, O. 2020. Effects of single and multiple species inocula of arbuscular mycorrhizal fungi on the salinity tolerance of a Bangladeshi rice (Oryza sativa L.) cultivar. Mycorrhiza. Doi: https://doi.org/10.1007/ s00572-020-00957-9. 30(4):431-444.
Porcel, R.; Aroca, R.; Azcon, R. and Ruiz, L. J. M. 2016. Regulation of cation transporter genes by the arbuscular mycorrhizal symbiosis in rice plants subjected to salinity suggests improved salt tolerance due to reduced Na+ root-to-shoot distribution. Mycorrhiza. 26(7):673-684. Doi: https://doi.org/10.1007/s00572-016-0704-5.
Ruiz. L. J. M.; Porcel R.; Azcon, C. and Aroca, R. 2012. Regulation of arbuscular mycorrhizae of the integrated physiological response to salinity in plants: new challenges in physiological and molecular studies. J. Exp. Bot. 63(11):4033-4044. Doi: https://doi.org/10.1093/jxb/ ers126.
Scagel, C. F.; Bryla, D. R. and Lee, J. 2017. Salt exclusion and mycorrhizal symbiosis increase tolerance to NaCl and KCl2 salinity in ‘Siam Queen’ basil. HortScience. 52(2):278-287. Doi: https://doi.org/10.21273/hortsci11256-16.
Sheng, M.; Tang, M.; Chen, H.; Yang, B.; Zhang, F. and Huang, Y. 2008. Influence of arbuscular mycorrhizae on photosynthesis and water status of maize plants under salt stress. Mycorrhiza. 18(6):287-296. Doi: https://doi.org/10.1007/s00572-008-0180-7.
Smith, S. E.; Facelli, E.; Pope, S. and Smith, F. A. 2010. Plant performance in stressful environments: interpreting new and established knowledge of the roles of arbuscular mycorrhizas. Plant and Soil. 326(1):3-20. Doi: https://doi.org/10.1007/s11104-009-9981-5.
Syvertsen, J. and Levy, Y. 2005. Salinity interactions with other abiotic and biotic stresses in citrus. HortTechnology. 15(1):100-103. Doi: https://doi.org/10.21273/horttech.15.1. 0100.
Yang, S. J.; Zhang, Z. L.; Xue, Y. X.; Zhang, Z. F. and Shi, S. Y. 2014. Arbuscular mycorrhizal fungi increase salt tolerance of Apple seedlings. Bot. Stud. 55(70):1-7. Doi: https://doi.org/10.1186/s40529-014-0070-6.
Yi, H.; Calvo, P. M.; MacKinnon, M. D. and Zwiazek, J. J. 2008. Responses of ectomycorrhizal Populus tremuloides and Betula papyrifera seedlings to salinity. Environ. Exp. Bot. 62(3):357-363. Doi: https://doi.org/10.1016/j.envexpbot.2007.10.008
Zwiazek, J. J.; Equiza, M. A.; Karst, J.; Senorans, J.; Wartenbe, M. and Calvo, P. M. 2019. Role of urban ectomycorrhizal fungi in improving the tolerance of lodgepole pine (Pinus contorta) seedlings to salt stress. Mycorrhiza. 29(4):303-312. Doi: https://doi.org/10.1007/ s00572-019-00893-3.
Descargas
Publicado
Cómo citar
Número
Sección
Licencia
Derechos de autor 2022 Revista Mexicana de Ciencias Agrícolas

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial 4.0.
Los autores(as) que publiquen en Revista Mexicana de Ciencias Agrícolas aceptan las siguientes condiciones:
De acuerdo con la legislación de derechos de autor, Revista Mexicana de Ciencias Agrícolas reconoce y respeta el derecho moral de los autores(as), así como la titularidad del derecho patrimonial, el cual será cedido a la revista para su difusión en acceso abierto.
Los autores(as) deben de pagar una cuota por recepción de artículos antes de pasar por dictamen editorial. En caso de que la colaboración sea aceptada, el autor debe de parar la traducción de su texto al inglés.
Todos los textos publicados por Revista Mexicana de Ciencias Agrícolas -sin excepción- se distribuyen amparados bajo la licencia Creative Commons 4.0 atribución-no comercial (CC BY-NC 4.0 internacional), que permite a terceros utilizar lo publicado siempre que mencionen la autoría del trabajo y a la primera publicación en esta revista.
Los autores/as pueden realizar otros acuerdos contractuales independientes y adicionales para la distribución no exclusiva de la versión del artículo publicado en Revista Mexicana de Ciencias Agrícolas (por ejemplo incluirlo en un repositorio institucional o darlo a conocer en otros medios en papel o electrónicos) siempre que indique clara y explícitamente que el trabajo se publicó por primera vez en Revista Mexicana de Ciencias Agrícolas.
Para todo lo anterior, los autores(as) deben remitir el formato de carta-cesión de la propiedad de los derechos de la primera publicación debidamente requisitado y firmado por los autores(as). Este formato debe ser remitido en archivo PDF al correo: revista_atm@yahoo.com.mx; revistaagricola@inifap.gob.mx.
Esta obra está bajo una licencia de Creative Commons Reconocimiento-No Comercial 4.0 Internacional.


